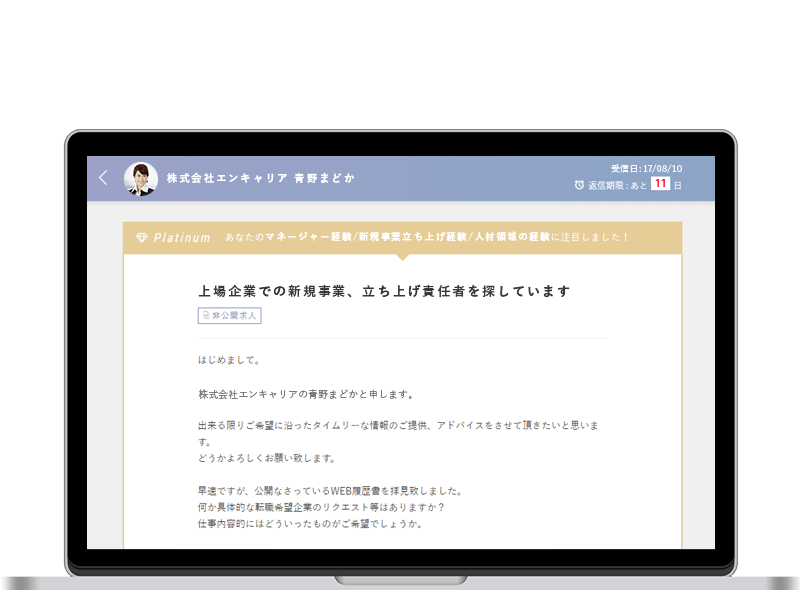
- どんな仕事か
-
<Overall Job Purpose>
? 医薬品の初期開発段階から承認取得までの期間を通し、開発薬事担当者として薬事戦略立案及び薬事的リスクマネジメントを行う。
? PMDAとの対面助言及び承認申請業務等、規制当局対応を薬事担当者の観点からリードする。
? Product Life Cycle Planの最大化に貢献する。
開発薬事は薬事手続き業務に特化した部署ではなく、薬事要件を考慮しながらよりチャレンジングな開発戦略を立案する部署であり、医薬品・医療機器開発の促進に関して重要な役割を担っています。
<Primary responsibilities>
? プロジェクトチームの代表として関係当局との交渉に責任を持つ。
? 開発早期からプロジェクトチームに参画し、薬事戦略の設定、それに基づく開発プランの作成において中心的な役割を果たす。
? Medical及びProject Management担当者等と協働し、Product Life Cycle Planの最大化に貢献する。
? Globalの薬事担当者と協同し、日米欧3極同時開発・同時申請・同時承認の達成をドライブする。 - 求められるスキルは
-
必須 <Required Experience>
医薬品開発における開発薬事担当者として3年以上の業務経験を有する者
<Essential Skills / license>
◆英語力(業務で英語を使っている) TOEIC730以上
◆情報などに基づいて、論理的な考えを明確に日本語と英語で表現出来る方
◆医薬品開発を通じて、規制当局との協働関係を築く事が出来る方
◆薬事環境の変化を察知する洞察力とその変化を業務に落とし込む企画と行動の出来る方
◆社内外の顧客及び米国本社の開発関連部署との効果的なコミュニケーション能力
<Desirable Experience>
◆海外勤務経験あるいはグローバルチームの一員として、開発プロジェクト参加経験
◆薬事担当者、開発企画担当者あるいは臨床開発担当者として、規制当局との交渉・折衝業務経験を有する方募集年齢(年齢制限理由) 45歳まで (長期勤続によりキャリア形成を図るため) - 雇用形態は
- 正社員
- どこで働くか
- 東京都/兵庫県
- 給与はどのくらい貰えるか
- 700万~1200万円程(スキル・経験により)
掲載期間17/08/30~17/09/12
求人No.EHRC-1116